2026年4月23日,北京大学未来技术学院分子医学研究所、北大-清华生命科学联合中心、生物膜国家重点实验室和麦戈文脑科学研究所周专实验室在Advanced Science发表了题为“A central somatic transmission mediates proprioceptive facilitation of muscle pain”的研究论文(网址:http://doi.org/10.1002/advs.202514242)。首次发现本体感觉通路中三叉神经中脑核(MeV)神经元通过非突触性的胞体分泌调控痛觉下行网络,介导慢性疼痛的长期维持。
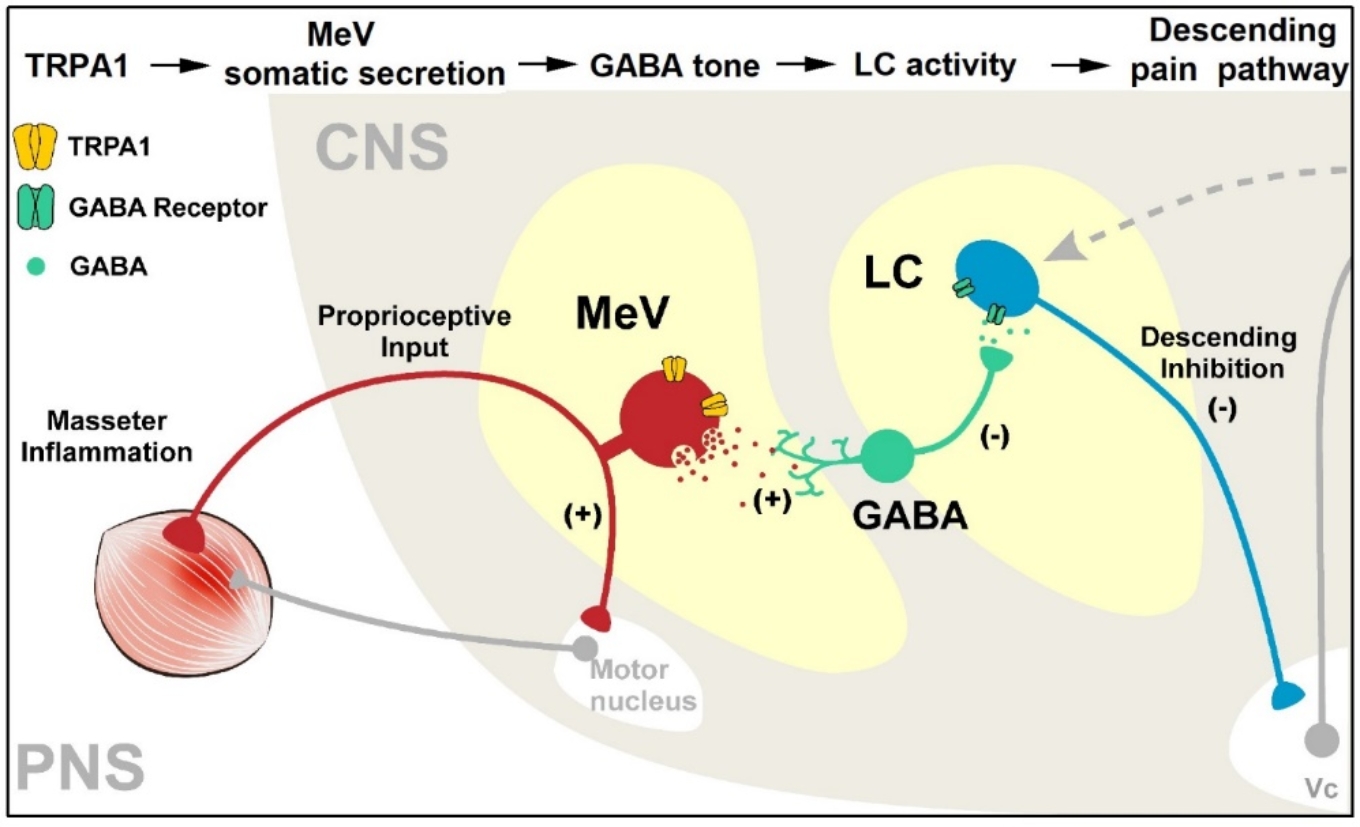
本体感觉(我们常说的“第六感”)负责感知机体姿势、运动及肌肉状态,而疼痛觉、触觉、温度觉是人体重要的躯体感觉系统, 分别负责感知组织损伤、机械刺激和温度变化。二者均是哺乳动物维持正常生命活动所必需的核心感觉功能。长期普遍认为这两类感觉系统分别依赖不同的外周传入纤维、中枢神经整合网络及传出通路,彼此相对独立运行。然而,临床发现在肌筋膜性颞下颌关节紊乱、特发性腰痛等慢性肌肉疼痛患者中,常伴随位置觉下降、肌张力失衡等本体感觉异常表现,提示两种感觉系统可能存在交互调控。 因此,两种感觉系统是否存在、如何交互调控及其生理/病理意义知之甚少。本研究发现,咬肌炎症可诱导脑干三叉神经中脑核(MeV)本体感觉神经元中TRPA1离子通道发生病理性敏化,触发MeV神经元胞体分泌,通过非突触性体积传递增强蓝斑核(LC)局部GABA能投射神经元的兴奋性,抑制蓝斑核去甲肾上腺素能(LC-NE)系统活性,削弱其下行镇痛调控功能,最终促进口颌面肌肉炎性痛的长期维持。
周专课题组在2012年发表在Journal of Physiology的工作首次在脑片水平上发现了MeV的胞体分泌现象;2016年发表在Journal of Cell Biology的工作揭示了TRPA1介导背根神经节神经元胞体分泌调控痛觉感知的外周机制;本项研究揭示了TRPA1介导MeV神经元胞体分泌调控下行镇痛系统的中枢机制,突破了神经元通讯主要依赖突触传递的传统认知,首次发现中枢神经元可通过胞体分泌实现跨细胞、跨核团的信息传递,不仅建立了“本体感觉—局部抑制网络—蓝斑核镇痛系统”全新脑干调控轴,为不同感觉系统的交互调控提供重要理论框架,还也为慢性肌源性颞下颌关节痛、功能性疼痛综合征等慢性痛干预提供了新靶点与新思路。
北京大学未来技术学院分子医学研究所张小玉博士(现北京大学口腔医学院助理研究员)、马里兰大学博士后杨佳乐和北京大学未来技术学院吴曦博士为本文共同第一作者。北京大学周专教授、马里兰大学牙医学院魏锋教授、北京大学口腔医院甘业华教授和西安交通大学王昌河教授为本文的共同通讯作者。北京大学分子医学研究所李杰博士、路福建博士等为本论文做出重要贡献。北京未来技术学院的程和平院士,复旦大学的黄志力教授、何苗教授和张玉秋教授,北京大学深圳研究院的张勃教授,加州福尼亚大学的David Julius教授,华盛顿大学的曹玉清教授和第四军医大学的王百忍教授为本研究提供了宝贵意见和帮助。该研究获得了国家自然科学基金、膜生物学国家重点实验室、IDG麦戈文脑科学研究所、北大清华生命科学联合中心等经费支持。
(生物物理与退行性疾病实验室供稿)


