Photonics Insights 2025年第1期封面:

【封面解读】
该封面展示了结构光照明显微技术(SIM)的基本光学原理及其在高时空分辨率活细胞成像中的应用。巧妙的 SIM 设计在高速光电调制器件赋能下使样本被具有特定光强分布的结构光快速动态激发,从而实现超越衍射极限的高时空分辨率成像。被照亮的高科技城市是细胞内部复杂动态结构的形象化展现:细胞核大楼、线粒体赛车场、内质网平台、高尔基体舞台和细胞骨架组成的交通网描绘了精彩的细胞世界和丰富的生命活动——SIM为活细胞内快速动态过程和精细机制的研究提供了强大工具,为生物学领域的创新突破创造了新的可能。
编者按
荧光显微技术作为探索生命奥秘的核心工具,长期面临着背景荧光干扰和光学衍射极限的挑战。结构光照明显微技术(SIM)作为超分辨技术的重要分支,通过引入时空编码的照明模式,不仅将分辨率提升至两倍衍射极限,更以“温和”(低光强、减少样本损伤)和“包容”(无需特殊标记和复杂处理)的独特优势,成为活细胞动态成像与复杂生物体系研究的新范式。
近期,北京大学席鹏教授团队应邀,在Photonics Insights 上发表题为“High Spatiotemporal Resolution Structured Illumination Microscopy: Principle, Instrumentation, and Applications”的综述论文,系统解析了SIM技术的原理、发展演进及应用前沿,并被遴选为2025年第1期“封面文章”。
文章从条纹干涉与点扫描两种机制出发,重点梳理了空间光调制器等高速器件对成像效率与灵活性的提升,并展望了其在疾病机制解析及细胞相互作用研究中的潜在应用。该综述不仅为生命科学研究者提供了重要的技术参考,也为初学者搭建了通往超分辨成像未来的桥梁,凸显出SIM技术在生命科学研究中革命性的应用价值与持续的创新趋势。
一、结构光照明显微技术的基本原理
顾名思义,结构光照明显微术是指以带有某种特定空间分布的照明光来激发样本荧光,也就是说,结构光是对样本真实空间信息的调制。在衍射受限的显微系统中,理想点光源的像被模糊成艾里斑,称为“系统的点扩散函数(PSF)”。PSF经傅里叶变换得到的频域结果就是系统的光学传递函数(OTF),它具有低通的特性,截止频率恰为衍射极限的倒数(图1 a, b)。SIM的基本原理在于高频的结构信息可以被低频的莫尔条纹所承载(图1 c),从而顺利地通过光学系统,被成像端采集并解出。
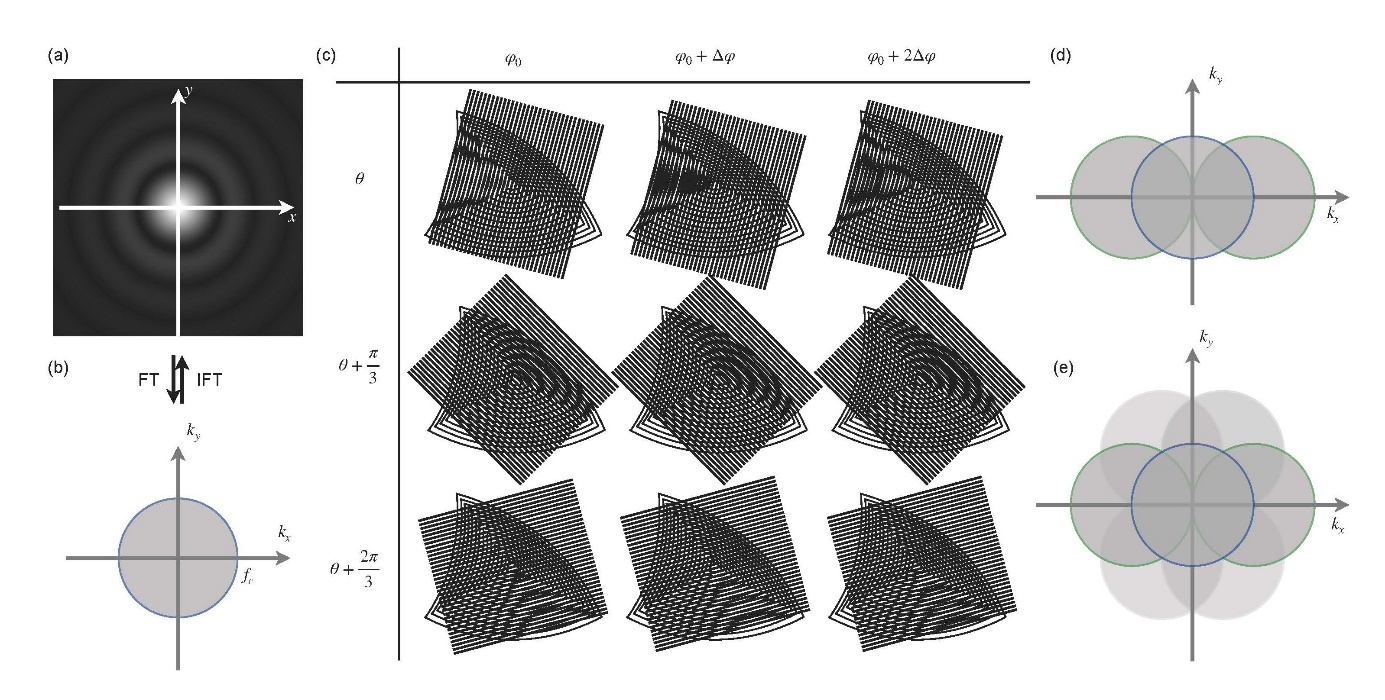
图1 a 理想点光源的像;b 光学传递函数;c 不同方向与相位的莫尔条纹;d 正弦条纹对频谱的扩展;e 可观测区域的各向同性扩展
最简单的结构条纹是正弦波。在正弦条纹的调制下,系统的频域可观测范围得到了提升,也就对应着更高的空间分辨率(图1 d)。旋转正弦条纹的方向,就能获得几乎各向同性的OTF扩展。
如果要在样本表面产生均匀的结构条纹,最基础和最重要的方法是光的干涉。相比于宽场荧光显微镜(图2 a),SIM用两束相干光入射物镜光瞳,就能产生特定频率的结构条纹。改变两束相干光的间距,还有可能进入全内反模态(TIRF),让正弦条纹仅出现在样本浅表而不再深入,从而得到更高的轴向分辨率和对比度(图2 c)。如果让三束光同时参与干涉,就能够在样本轴向也产生结构条纹,从而以类似的原理获得轴向分辨率的提升(图2 d)。
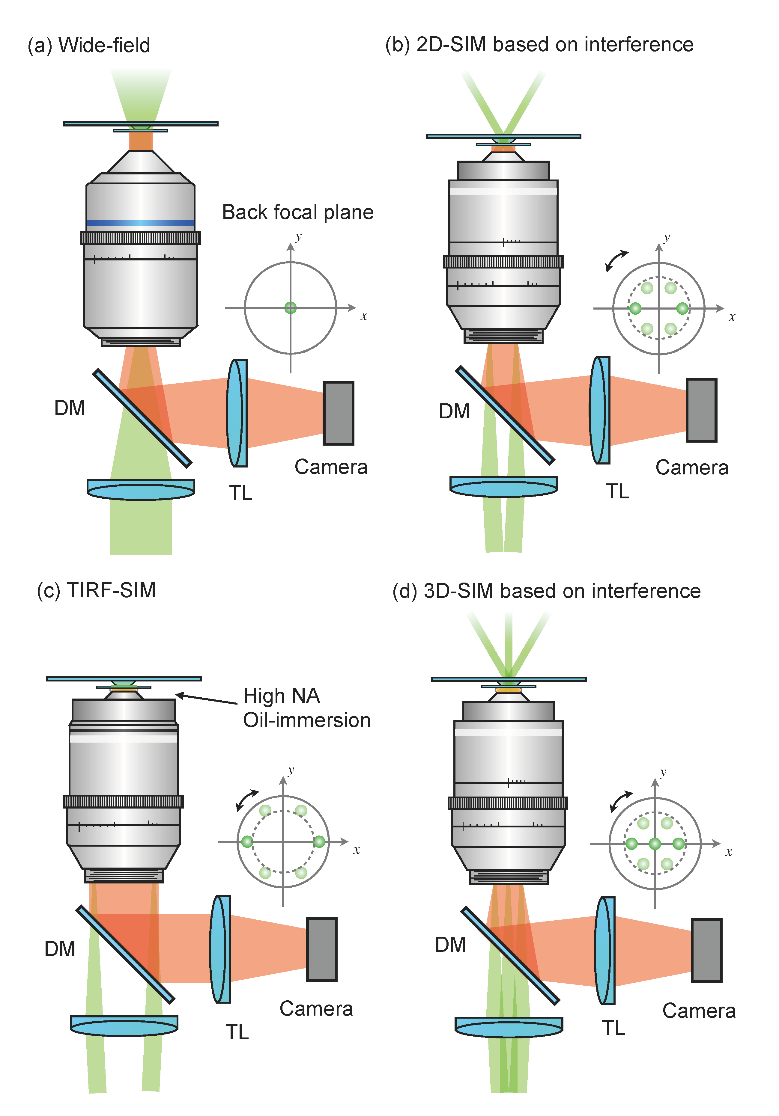
图2 a 宽场荧光显微镜;b 2D-SIM;c TIRF-SIM;d 3D-SIM
除了条纹之外,在样本平面上扫描的聚焦光点(或光点阵列)也可以看作结构照明光。一对共轭的聚焦小孔可以让系统获得理论上1.41倍的分辨率提升——在此基础上进行高速成像与重建成为点扫描SIM技术发展的主线。
二、结构光照明显微镜的实现与技术进展
光照模式的精确控制是SIM实现的关键,其切换速度和精度直接影响成像的时空分辨率。衍射光栅是基于条纹的SIM技术的核心元件,其±1级衍射光束通过干涉生成周期性的正弦条纹。结构光图案的旋转和相移依靠光栅的旋转与平移实现,成像速度受到较大限制。点扫描SIM技术的时空分辨率主要受原始图像的数量以及聚焦点的精确步进等因素影响。
随着空间光调制器(SLM)、数字微镜阵列(DMD)和振镜(Galvo)等高速光调制器的快速发展,SIM的时空分辨率得到了显著提升。
在基于条纹的SIM技术中,SLM通过电子控制生成像素化的光栅图案,能够快速切换光的方向和相位,显著提高了成像速度和分辨率(图3 a)。DMD作为一种新型的高速光调制器,具有较高的开关频率,且能在不断刷新图案的情况下稳定工作,其低成本和高效率使其在SIM中逐渐获得应用(图3 b)。基于扫描振镜的SIM系统通常采用两个完全对称的扫描单元,通过精确控制激光的扫描路径和频率实现高速SIM成像(图3 c)。
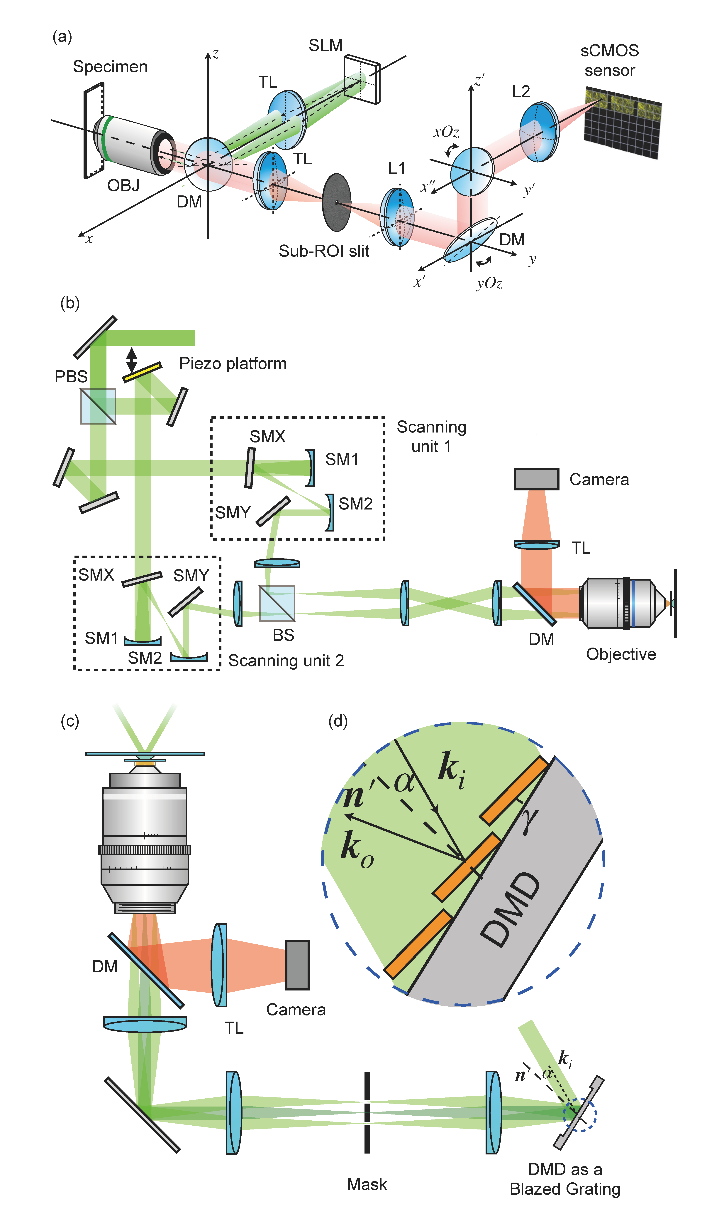
图3 基于条纹的SIM实现方式。a 基于SLM的SIM系统;b 基于振镜的SIM系统;c 基于DMD的SIM系统
在点扫描SIM中,需要精确且快速地控制激光扫描,常用的器件包括DMD、振镜和转盘。DMD在点扫描SIM中用于生成稀疏的二维激发图案,并通过步进扫描实现高效成像(图4 a)。结合数字定位和解卷积技术,能够有效提高成像速度并减少数据量。
扫描振镜则通过对发射荧光进行重扫描,实现光子的重分配,从而减少数据处理的需求(图4 b)。转盘通过其高速扫描特性和微透镜阵列的组合,在快速扫描样品的同时,增强了光的使用效率,进一步提升了时间分辨率(图4 c)。高速光调制器的广泛应用使得SIM系统的时空分辨率得到极大提升,为结构光显微技术的发展提供了强有力的推动力。
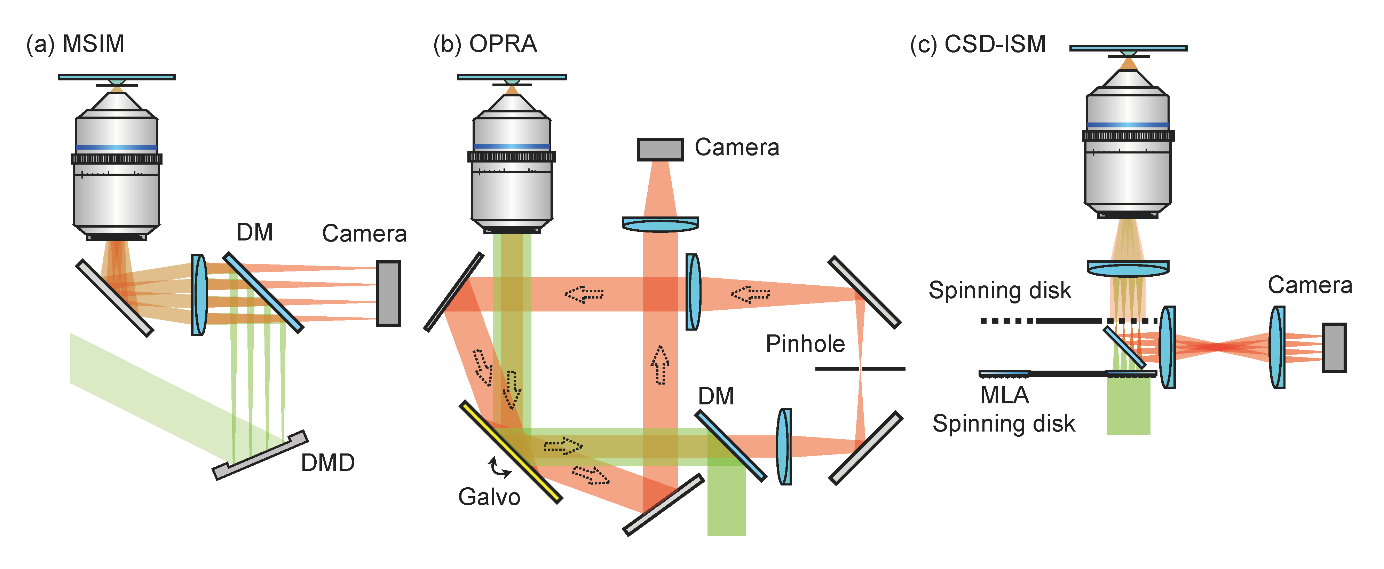
图4 点扫描型SIM的实现方式。a 基于DMD的点扫描SIM系统;b 基于振镜的点扫描SIM系统;c 基于转盘的点扫描SIM系统
三、结构光照明显微技术在生物学前沿的应用与突破
与传统荧光显微镜相比,SIM突破衍射极限实现了两倍分辨率的提升,凭借其高时空分辨率和低光毒性在生物学研究领域脱颖而出,成为最流行的超分辨显微技术之一。
SIM技术能够显著提高生物结构的成像清晰度。通过SIM,研究人员得以观察细胞与病毒之间的相互作用,为揭示病毒致病机制提供重要线索(图5 a)。此外,非线性SIM技术的成功应用,使得核孔复合物的环状结构得以清晰分辨,F-肌动蛋白等精细复杂的细胞结构也得到了清晰成像(图5 b)。
SIM非常适合进行活细胞成像。SIM技术已成功应用于线粒体的动态变化观察,如线粒体的分裂、融合等过程(图5 c)。甚至更为复杂的内质网小管收缩也能被清晰捕捉,为细胞动力学研究提供了强有力的工具(图5 d)。
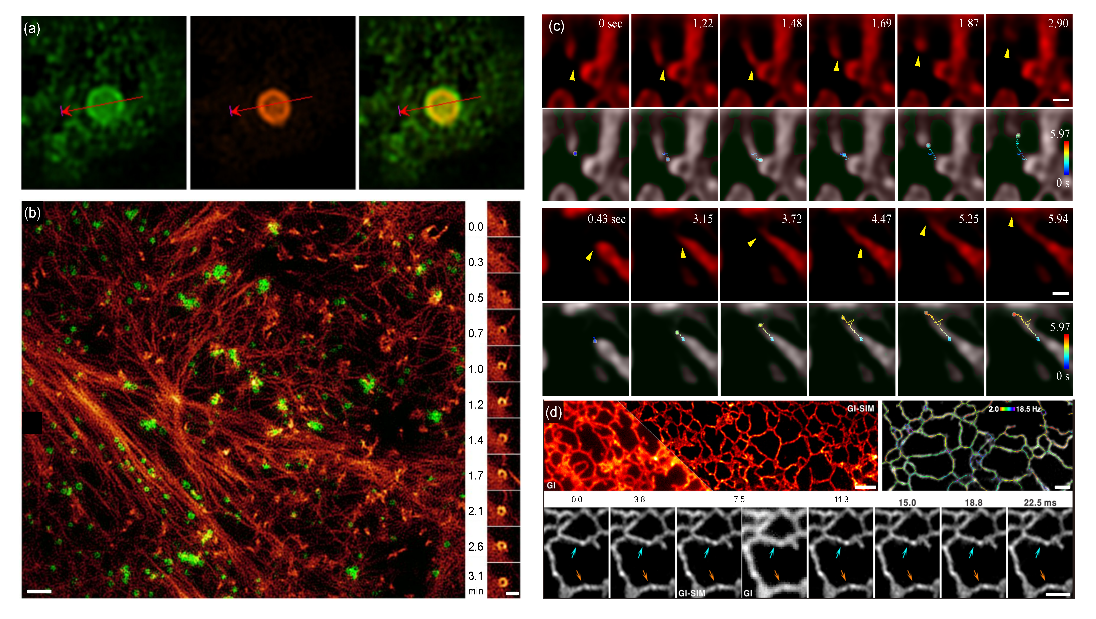
图5 SIM以高时空分辨率揭示亚细胞结构和动态过程,a SIM观察到的JC病毒感染的人胶质细胞中PML-NB的精确组织;b F-肌动蛋白形成了一个纳米环;c 线粒体“kiss-and-run”和“extrusion”事件的伪彩色轨迹;d COS-7细胞内质网小管收缩
SIM的多色成像能力为揭示细胞器间的动态交互提供了重要支持。借助多色SIM技术,研究人员已经揭示了线粒体与溶酶体(图6 a)、线粒体与微管、线粒体与内质网、内质网与囊泡以及微管与肌动蛋白等细胞器之间的相互作用,进一步加深了我们对细胞器功能及其相互作用在细胞调控中的作用的理解。
在三维成像方面,SIM展现了出色的能力,能够深入观察厚样本中的细胞结构。例如,MC-ISM技术成功实现了植物细胞中线粒体的三维成像,揭示了植物和动物细胞线粒体的相似性(图6 b)。通过结合适应光学与多焦点结构光照明显微技术,研究人员还能够在更深层次的组织中进行动态观察,揭示神经发育过程中轴突延伸与突触形成等关键过程(图6 c)。
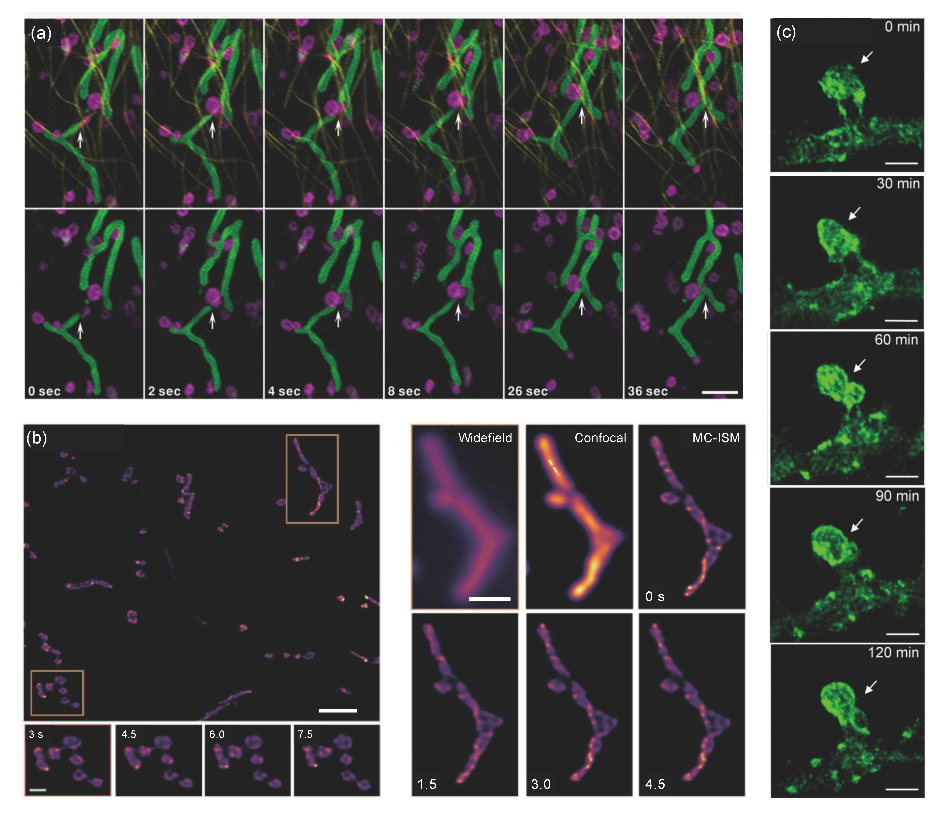
图6 SIM观测到的细胞器互作多色成像及更大深度的成像,a 线粒体与溶酶体互作的过程;b 拟南芥下胚轴条状和球状线粒体成像结果;c 轴突的动态形态学变化
四、总结与展望
近年来,SIM在生物医学领域的重要性日益凸显,已成为研究细胞功能与结构的关键工具。针对SIM成像的特性,该综述对经典SIM成像系统的多方面性能进行了综合评估,并通过雷达图的方式帮助研究人员根据自身需求选择最合适的技术方案(图7)。
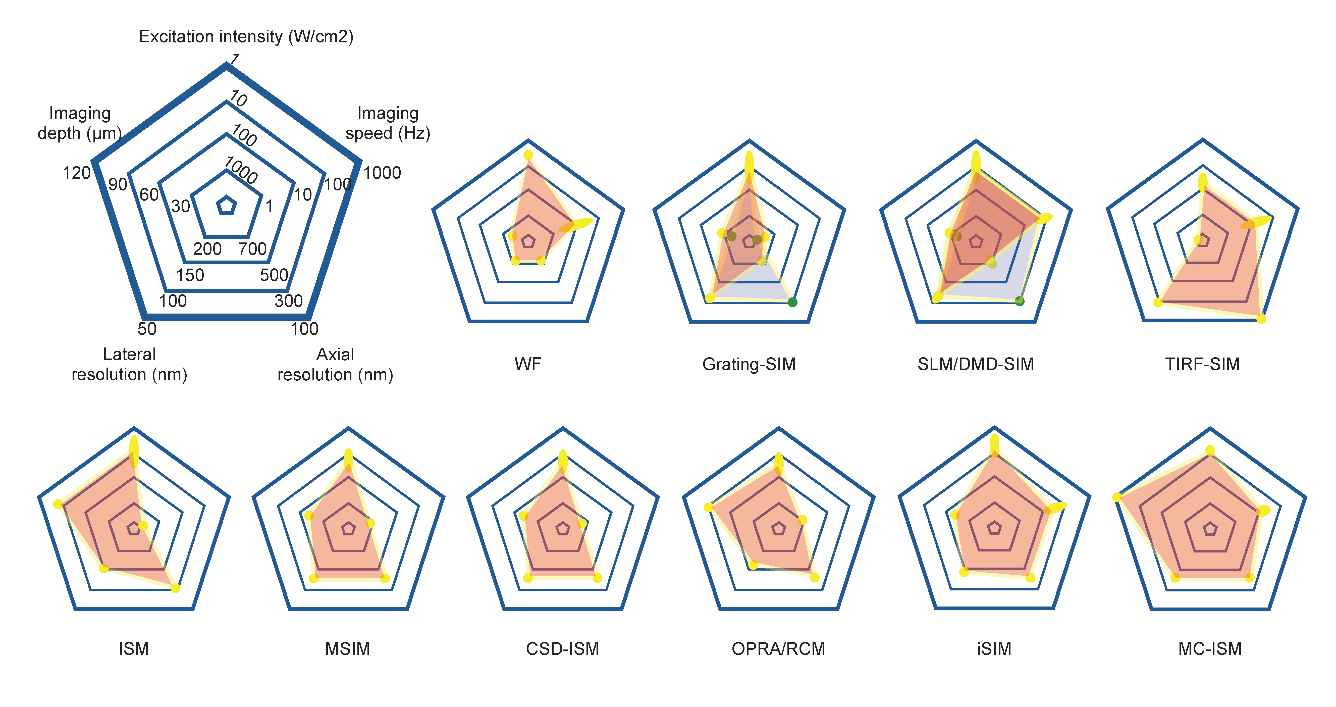
图7 SIM技术性能比较的雷达图(浅蓝色部分和绿色点代表在3D成像模式下的表现)
随着生物研究对高分辨率成像需求的不断增加,SIM技术也在不断与其他显微技术相结合,以提升其综合性能。例如,SIM与电子显微镜、定量荧光共振能量转移等技术的结合通过原理上的互补,提供了更强大的成像能力。此外,SIM与无标记成像技术,如三维光学衍射层析成像的结合,为活细胞成像提供了更加深入的分析能力,同时减少了光毒性,进一步拓展了其应用范围。
展望未来,SIM的技术发展将涵盖多平面并行成像、偏振SIM等新兴成像方式。这些创新将进一步扩展SIM在生命科学领域的应用边界,推动细胞机制与疾病研究的深入发展。随着对生物学知识探索的不断深入,SIM有望进化为更强大的超分辨率成像工具。在不久的将来,SIM与其他成像模式的协同应用有望揭示更复杂的亚细胞结构和动态过程,为生命科学领域带来更多突破。
科学编辑 | 北京大学 王瀚、王文姝
编辑 | 方紫璇
作者简介:

席鹏,北京大学未来技术学院博雅特聘教授,国际先进材料学会会士(FIAAM),国家杰出青年科学基金获得者,科技部重点研发计划首席科学家。主要从事超分辨显微成像技术的研究。现担任Advanced Photonics、Light等5种国际学术期刊的编委。在Nature、Nature Methods等国际一流期刊发表SCI收录期刊论文100余篇,总影响因子大于850,被引超过6000次。2016年获得中国光学重要成果奖。2022年获得广东省自然科学二等奖(排名第二)。已授权美国专利4项,中国专利19项,编辑专著2部。多次被OPTICA(原OSA)和SPIE组织的国际会议邀请作大会邀请报告。

李美琪,2022年获得北京大学理学博士学位,师从席鹏教授。现任北京大学生命科学学院工程师,主要研究方向为超分辨荧光显微成像,以(共同)第一/通讯作者在Nature Communications, eLight, The Innovation,PhotoniX等期刊发表论文11篇。在国内开设了《生物荧光成像实验》课程,首次将超分辨荧光显微镜搭建引入大学课堂,曾获北京大学第二十三届青年教师教学基本功大赛一等奖,第十三届创新教学应用大赛一等奖等多项教学奖项。主持/参与国家自然科学基金青年基金,重点项目等各类基金项目6项。

王瀚,北京大学未来技术学院生物医学工程系博士研究生,师从席鹏教授。2024年本科毕业于东南大学吴健雄学院。

王文姝,北京大学未来技术学院生物医学工程系博士研究生,师从席鹏教授。本科毕业于哈尔滨工业大学威海校区。
