近日,北京大学未来技术学院程和平课题组在 Basic Research in Cardiology (https://link.springer.com/article/10.1007/s00395-023-01015-z)上发表最新研究成果,揭示了线粒体内膜上的琥珀酸脱氢酶(SDH)在心脏表观遗传和代谢稳态中的调控机制,并研究了心肌病中SDH的致病机理和潜在的治疗方法。
脂肪酸被认为是成年健康心脏的主要能量来源。脂肪酸氧化(FAO)约占心肌能量需求的 70%。心力衰竭的一个标志是代谢从脂肪酸氧化转变为糖酵解。然而,心肌代谢转换的具体机制仍有待充分了解。
在本研究中,作者发现定位于线粒体内膜的琥珀酸脱氢酶对于维持FAO/糖酵解的心脏稳态至关重要。临床数据显示,SDH亚基上多个位点的突变均可引发严重的扩张性心肌病,并导致心衰致死。作者首先构建了心肌细胞特异的SDH亚基突变小鼠,SDH功能缺陷的小鼠同样出现扩张型心肌病的表型和心力衰竭。接下来,作者揭示了SDH调控心肌病的分子机制:SDH缺陷引起心肌细胞琥珀酸的累积,从而引起细胞核内全基因组水平的DNA过度甲基化,这种表观遗传重塑进一步抑制了FAO相关基因的转录,降低了脂肪酸的代谢能力;相反的糖酵解代偿性升高,最终改变了心肌代谢的稳态。
作者还发现高脂肪饮食(HFD)可以增加动物体内的脂肪酸供应,增强心肌细胞的FAO水平,缓解心衰的症状。另外,琥珀酸的竞争性抑制物α-酮戊二酸也可以抑制心衰中的DNA甲基化,逆转上述变化并改善心肌病动物的心脏功能(图1)。
此项研究揭示了SDH在衰竭心脏代谢重塑中的重要作用,并探索了在SDH突变引起的心肌病中保护心脏的治疗策略和干预方法。程和平教授的毕业生李雯雯博士为论文的第一作者,课题组马淇博士为该论文的通讯作者。该课题还得到未来技术学院代谢组学平台、南开大学陈佺教授的支持和帮助。该研究获得了国家自然科学基金和生命科学联合中心的资助。
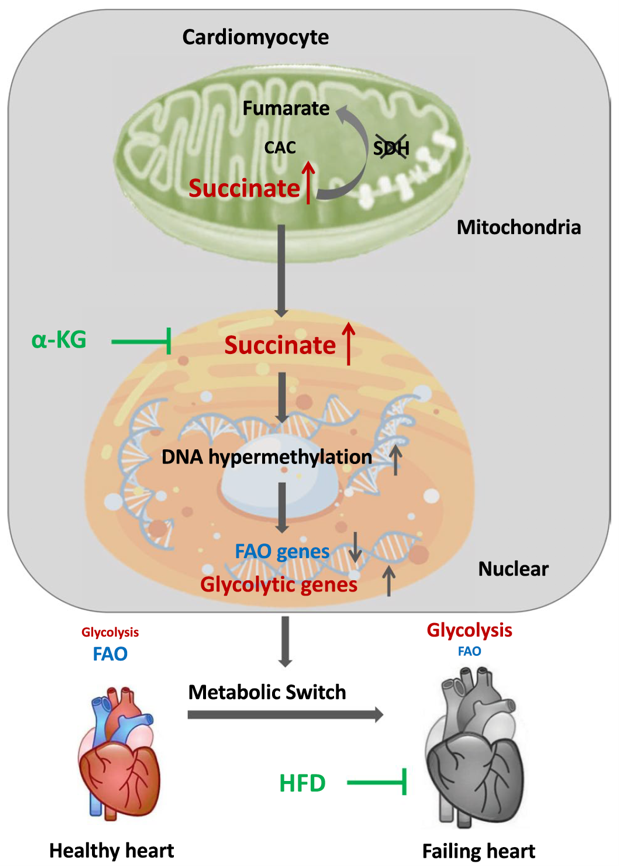
图1,琥珀酸脱氢酶调控心脏功能的模式图。线粒体内膜的琥珀酸脱氢酶突变,可以引起心肌细胞中琥珀酸的累积,诱导细胞核内的表观遗传重塑和甲基化水平增多,导致心脏代谢重编程和心衰。
